
文章图片

文章图片

文章图片

文章图片

文章图片

文章图片
文章图片
类器官(Organoids)是一种类似于组织器官 , 由不同类型干细胞加入相应培养基配方 , 通过某种支持介质在体外细胞培养系统制备 , 产生类似体内器官结构和功能的三维“微器官模型” 。
与传统仅能得到单层细胞的二维培养模式相比 , 通过三维培养能得到具有立体空间结构 , 涵盖多种类型且成熟度较高的细胞 , 所形成的“微器官”具有功能性 , 能在体外模拟器官组织的发生过程及生理病理状态 。 因而在疾病模型建立、药物毒理筛选、基因和细胞疗法服务等领域具有广阔的应用前景 。
△ 类器官的产生和治疗潜能
类器官技术的诞生 , 无疑为科学家研究各种组织的功能提供了更为强大的工具 。
为构建类器官与原生组织结构的相似性 , 其培养重要条件之一:干细胞或器官祖细胞的发育 , 对类器官的培养尤为重要 。
由日本Shinya Yamanaka团队开发 , 于2012年获得诺贝尔奖技术的诱导多能干细胞(iPSCs) , 是一种利用编码转录因子四种特定基因引入成熟体细胞 , 实现重编程为无限繁殖、在体内具有产生所有细胞类型的多能干细胞 。 其相比胚胎干细胞能完美绕开 “伦理之争” , 同时又兼具与自体匹配干细胞系无限繁殖、多向分化潜能 。 因而 , iPSCs已成为类器官培育主要的组织干细胞来源 。
△ iPSC构建类器官培养体系
目前 , 基于iPSCs类器官技术已成功培养出大量具有部分关键生理结构和功能的类组织器官 , 如肾脏、肝脏、肺、肠、大脑、前列腺、胰腺和视网膜等 。
神经系统疾病由于发病机制及治疗范围有限 , 与其他疾病领域相比 , 药物治疗改进效率依然较低 。 随着干细胞技术发展与推广 , 培养人大脑类器官成为目前神经科学研究领域炙手可热的研究项目 。
人脑类器官(human brain organoids)是iPSCs在模拟大脑发育环境培养液中分化产生的类似人脑三维组织 。 在结构中 , iPSC诱导为拟胚体 (Embryoid Body EB) , 在外胚层形成后 , 引导分化为神经或非神经方向 。 引导分化法获得类器官依赖分化过程中添加的生长因子 , 得到脑区特异性的区域如皮层、海马、中脑、大脑 。 引导分化法得到的类器官含有神经祖细胞、神经元、星形胶质细胞及其他大脑细胞 。
△ 人脑类器官培养方法 , 培养皿中“人类大脑” , 发育似5周婴儿
2021年3月 , 加州大学洛杉矶分校Daniel H. Geschwind教授和斯坦福大学Sergiu P. Pa?ca教授 , 在Nature Neuroscience发表最新成果 , 建立可长时间培养 , 具有自我成熟能力的大脑类器官 , 其中关键基因 , 蛋白 , 表观遗传等变化 , 基本完全模拟胎儿直至产后的大脑皮质发育过程 。
△ Nature Neuroscience研究成果发表
加州大学和斯坦福大学的科学家创新性地开发了可以自我成熟大脑皮质类器官 , 能够使用离体模型模拟体内神经发育过程 , 为研究神经发育不全、精神类疾患、神经退行性疾病等 , 提供了仿真的研究工具 。
△ 该试验大脑类器官培养过程
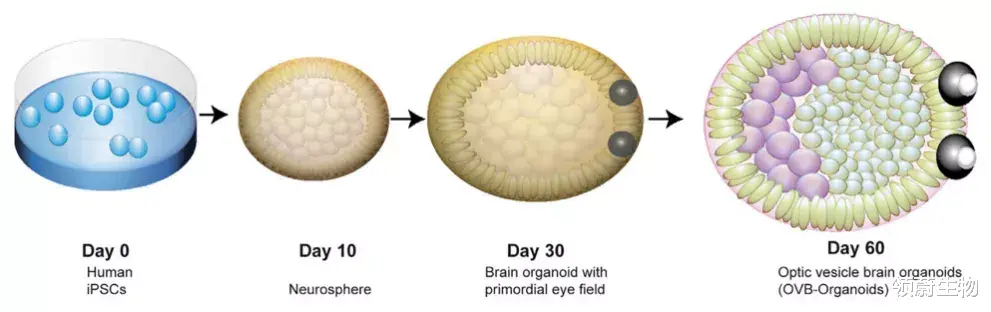
随着技术发展 , 诸多团队尝试用不同方法培养脑区特异性类器官后将其共培养 , 以得到更完善的脑组织 , 使之会自我融合形成含有不同脑区的类器官模型(如眼睛) , 从而用于研究脑各区间的相互作用 , 以便全方位研究类人脑三维组织的发育、疾病或药物效果 。
作为人脑在胚胎发育重要部分之一 , 眼睛的发育是一个非常复杂的过程 。 现阶段虽已有利用iPSC成功诱导出纯粹的视网膜类器官可以组装视泡样结构 , 但其功能和结构与在体内正常发育的视泡相差甚大 。
推荐阅读
- 它们的智商已经高到人类无法理解,即使还没有爬到食物链顶端!
- 揭秘陶乐德事件:男子在拘留室离奇消失,难道平行时空真的存在?
- 青藏高原将停止增高,后果不可承受,我们却未感到危机
- 人类还会再进化吗?会进化成什么样子?
- 寻求气候变化的确定性:要多少才足够?
- 少见!今年十五的月亮,不是十六圆
- 科学家在大型强子对撞机上寻找难以捉摸的基本粒子
- 为人类敲响警钟!57000年前的尸体重见天日,史前生物现身引发关注
- 地球果真出了大问题?火山爆发后出现神秘现象,科学家紧急发声
- 简述相对论发展史:从伽利略到引力波







