2022年1月10日 , 在拿到广州首张新冠mRNA疫苗临床批文两个月后 , 广州锐博生物科技有限公司(下称“锐博生物”)和阿格纳生物制药有限公司(下称“阿格纳制药”)在成都正式启动自主研发的新冠mRNA疫苗I期临床试验 。 从启动研发到进入临床 , 这一路扎实地走了整整两年 。
“从目前完成的低剂量临床试验来看 , 没有一例出现发烧反应 , 说明疫苗的安全性很好 。 ”近日 , 锐博生物和阿格纳制药董事长张必良接受南都采访人员专访时透露了这一消息 , 更令人振奋的是 , 根据稳定性研究结果 , 该款新冠mRNA疫苗可在2-8℃常规冰箱中储存12个月 , 活性依旧稳定 。
此款新冠mRNA疫苗的特点何在?临床预期计划如何?是否能应对现阶段出现的变异毒株?锐博生物即将试投产的寡核苷酸药物和mRNA创新性疫苗研发及生产基地 , 又将如何加快新冠mRNA疫苗的上市之路?……张必良逐一解开了南都采访人员的若干疑问 。

文章图片
广州锐博生物和阿格纳制药董事长张必良 。 受访者供图
人物名片:
张必良:美籍华人 , 广州市锐博生物科技有限公司董事长 , 中科院广州生物医药与健康研究院研究员、博导 。 在美国哥伦比亚大学获有机化学博士学位 , 后在美国科罗拉大学化学系从事博士后研究 。
曾任美国麻省大学医学院分子医学系和生物化学与分子药理系研究室主任 , 主要从事 RNA 化学生物学研究包括小干扰 RNA(siRNA)及微 RNA(miRNA) 的研究和产业化 。 他是世界上首次发现核酶催化肽键合成 , 并确立了 RNA 在生命过程中以及在物种起源和进化过程中的重要地位 。
以全长S蛋白为抗原
2-8℃常规冰箱中可储存12个月
南都:锐博生物研发的新冠mRNA疫苗为何选择走全长S蛋白的技术路线?
张必良:我先介绍一下 , 锐博生物是一家以核酸技术为核心的国家火炬计划重点高新技术企业 , 主要从事寡核苷酸产品研发和生产 。 新冠mRNA疫苗是一种核酸疫苗 。 2020年1月 , 在广东省政府部门组织下 , 由锐博生物来牵头 , 联合中科院广州生物医药与健康研究院和阿格纳制药共同开展新冠疫苗应急攻关项目科研合作 , 并成立了研发攻关团队 。
由于前期我们对新冠病毒(SARS-CoV-2)了解十分有限 。 经过多个月筛选研究 , 开发了多款能产生免疫原性和中和抗体的mRNA候选疫苗 。
新冠病毒有10多个蛋白可能是疫苗的候选靶点 , 对于究竟选哪一个作为抗原 , 我们也做了很多前期筛选 。 到了2020年2月下旬 , 《Science》期刊上发表了一篇S蛋白晶体结构的文章 , 指出S蛋白是病毒宿主细胞受体介导病毒入侵的关键蛋白 , 预融合构象结构所产生的抗体能更好地保护受体 。 我们就通过大规模的动物免疫试验 , 对S1蛋白、S2蛋白、RBD、和全长S蛋白都做了免疫原性研究 , 最终发现还是全长S蛋白抗原的免疫原性更高 。 我们才选定全长S蛋白作为抗原 。
(注:新冠病毒(SARS-CoV-2)有四种主要的结构蛋白 , 分别是刺突蛋白(S蛋白)、核衣壳蛋白(N蛋白)、膜蛋白(M蛋白)、包膜蛋白(E蛋白) 。 S蛋白为新冠病毒粒子外膜表面的刺突 , 有S1、S2两个亚基 , RBD位于S1亚基上 , 负责和人体细胞ACE2结合 。 )
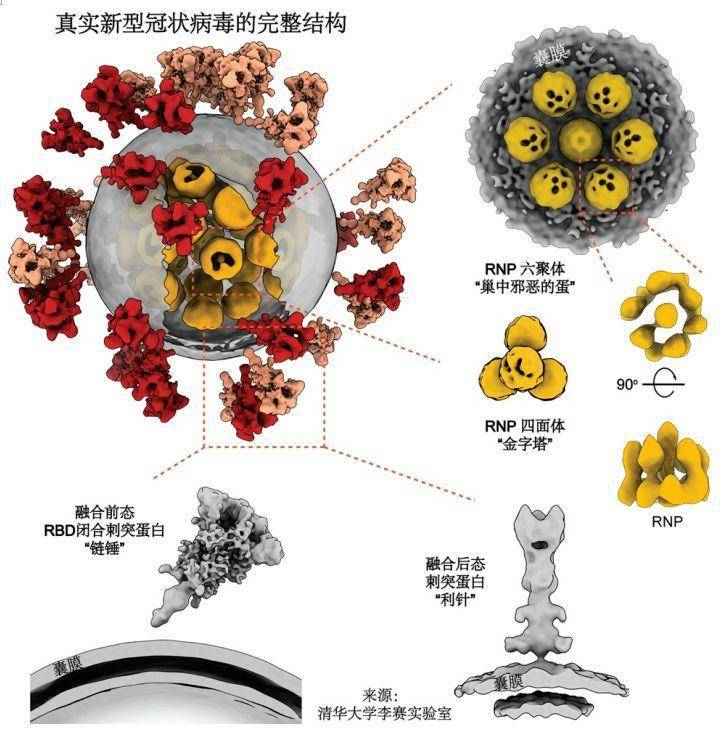
文章图片
真实的新冠病毒全病毒内外结构图 。 图片来源:清华大学李赛实验室
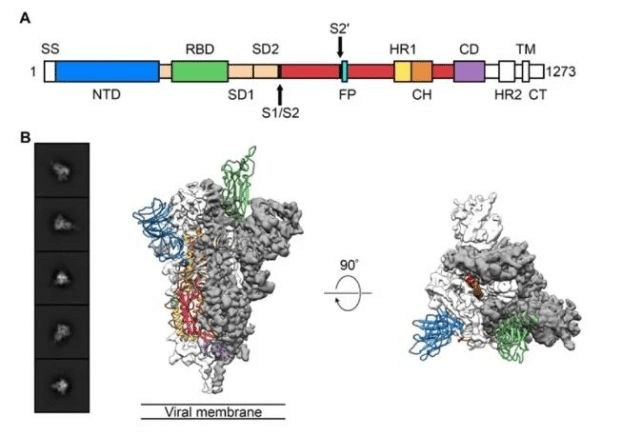
文章图片
新冠病毒S蛋白的三聚体结构 。 图片来源:BioRxiv
南都:这款新冠mRNA疫苗有什么特点?
张必良:我们的mRNA疫苗可以像灭活疫苗一样保存在2-8℃的常规冰箱中 , 稳定性研究从去年春节至今已经持续12个月 , 疫苗活性保持一致 , 这是突出特点;另外 , 这款mRNA疫苗是预融合稳定构象结构的设计 。 (注:由于mRNA疫苗具有不稳定性 , 有mRNA疫苗须储存在-80℃至-60℃的超低温冰箱中 。 )
此外 , 这款疫苗原液mRNA纯度超过95% , 特异性结合抗体IgG滴度可达百万以上 , 中和效价达到1000-5000 。 疫苗偏好Th1型的T细胞免疫应答 。
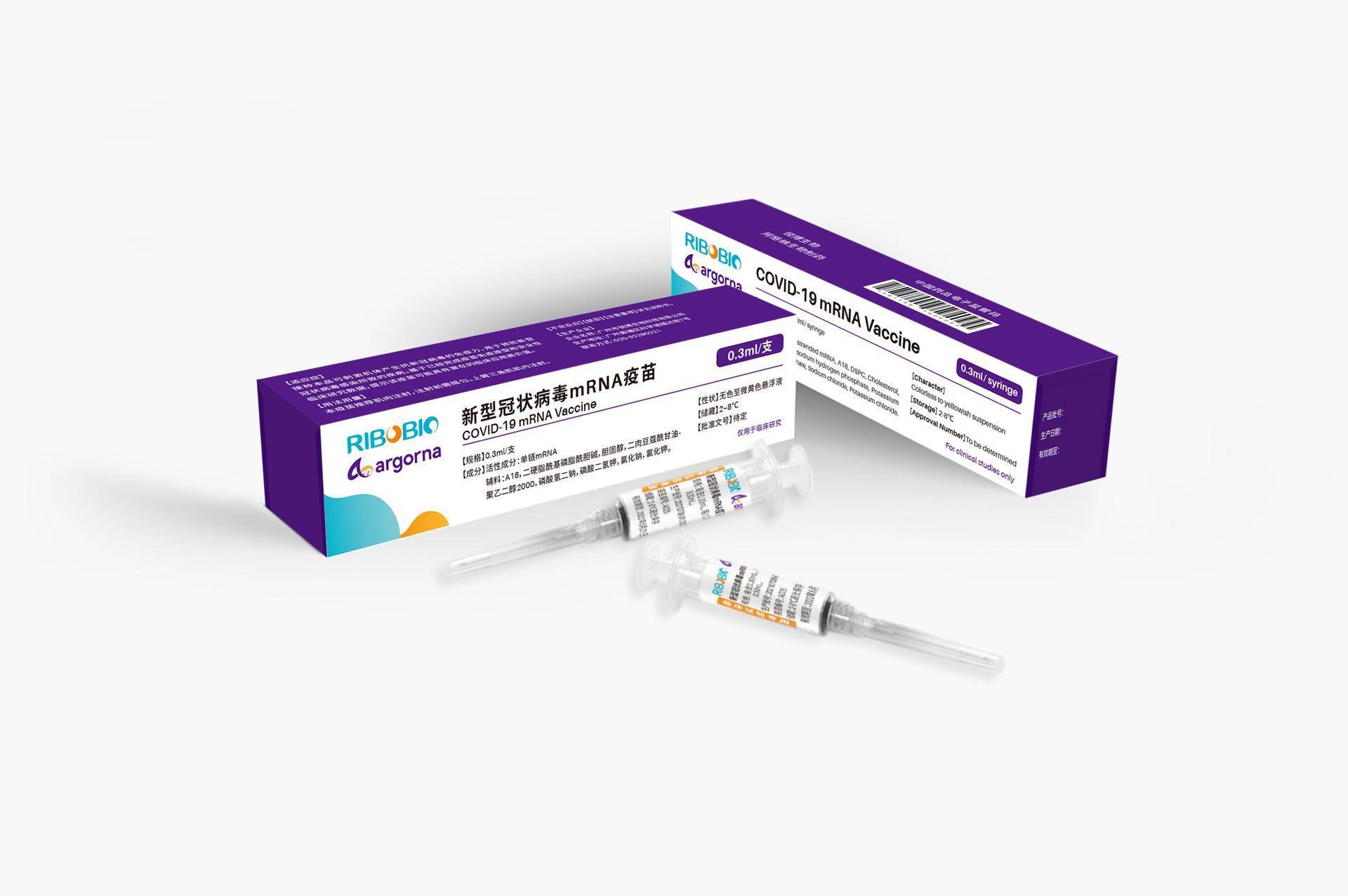
文章图片
锐博生物自主研发的新冠病毒mRNA疫苗产品图 , 仅用于临床研究 。 受访者供图
南都:如何判断疫苗的稳定性?
张必良:这一年来 , 我们开展了疫苗的稳定性研究 , 12个月后疫苗所有性能指标都达到相关质量标准 。 并且 , 我们必须做生物活性检测 , 就是注射到小鼠体内后是否能产生抗体 , 以此判断疫苗的稳定性 。 这些稳定性数据已提交至中检院 。
Ⅰ期临床显示疫苗安全性优越
尚未出现发热反应
南都:疫苗Ⅰ期临床测试于今年1月10日正式启动 , 目前已满一个月 , 有什么进展可以透露?
张必良:Ⅰ期临床主要为疫苗安全性研究 , 做剂量爬坡 。 我们分了成人组和60岁以上老人组两个大的组别 , 其中成人组又分低、中、高剂量三个组别 , 老人组分低、中剂量两个组别 , 总共120例受试者 。
新冠mRNA疫苗是一项新兴技术 , 开展临床研究需要先做“哨兵”试验 。 也就是一组受试者要接种疫苗 , 先挑出4例先接种疫苗 , 这4例就是“哨兵” ,“哨兵”打完后未发现安全性问题 , 再接种剩下受试者 。 先开展低剂量测试 , 目前(截至2月11日)已完成低剂量成人组、中剂量成人组“哨兵”和低剂量老人组“哨兵”的接种 。 低剂量成人组已经接种了第2针 , 都未出现发烧反应等副作用 , 说明疫苗安全性很好 。
南都:Ⅰ期临床为何选择在成都而不是广州?
张必良:一般情况下 , 疫苗临床试验都是在CDC(疾病预防控制中心)开展 , 但新冠mRNA疫苗与传统疫苗不一样 , 需要在医院开展临床研究 。 我们当时联系了很多家第三方服务单位 , 广东能开展临床研究的点不多 , 而且Ⅰ期临床必须要找到一批从未打过疫苗的健康人 。 成都还能找到受试者 , 并且可以很快帮助我们入组 , 所以就选择了成都开展临床试验 。
南都:我们曾了解到 , 在疫苗研发阶段 , 动物攻毒试验资源短缺是当时锐博生物面临的最大困难?
张必良:在疫苗项目开发早期阶段 , 疫苗的动物攻毒试验要用恒河猴一类的大动物进行 , 国内能开展大动物攻毒试验的机构很少 , 资源十分短缺 。 我们当时选择了中国科学院武汉病毒研究所 , 一切准备就绪 , 原计划2020年9月开展攻毒试验 , 但病研所反馈资源紧张 , 推迟到了11月份进行 , 2021年初提供病理分析数据后 , 我们才将材料送至CDE(国家药品监督管理局药品审评中心)进行临床研究申报 。 到2021年11月获得CDE签发《药物临床试验批件》 , 是广州第一个新冠mRNA疫苗临床批文 。
不过 , 在那两个月等待过程中 , 我们委托广州海关P3实验室和广州市呼吸健康研究院做了小动物攻毒试验 , 结果显示疫苗的保护效果很好 。 这个数据我们也上报了CDE 。
一代疫苗Ⅱ期临床预计4-5月份完成
三代苗对目前所有变异株有效
南都:新冠病毒株的快速变异 , 会否让您有强烈的紧迫感?
张必良:当然!目前国外已上市的新冠mRNA疫苗已经注射了三十亿剂以上 , 我们国产的新冠mRNA疫苗还未上市 。
好在mRNA疫苗产品具有开发和生产快的特点 , 依托病毒的测序序列就可以快速设计出疫苗抗原 , 进入动物实验和临床前研究 。 一个全长S蛋白的mRNA序列将近4000个核糖核苷碱基 , 我们只要把发生突变的位点进行编辑修改 , 就能开发出一个针对变异株的新疫苗 。 例如 , 奥密克戎变异株共携带超过50个突变而S蛋白上的变异位点达32处 , 就需要将这些发生突变的位点改掉 , 而疫苗的生产工艺和成分都一样 。
相较之下 , 研发灭活疫苗需要花一定时间分离得到病毒株 , 再经过长时间的细胞培养获得灭活疫苗 。
南都:所以锐博生物的新冠mRNA疫苗研发也在不断升级?
张必良:现在在成都进行临床试验的是一代疫苗 。 有了一代苗后 , 我们很快研发出了针对德尔塔病毒的二代疫苗 。 去年11月20日公布了奥密克戎变异株 , 我们在一个月后(12月20日)就研发出了针对奥密克戎的三代疫苗 , 目前正在进行攻毒试验 。 可以说 , 我们只要有一款疫苗获批上市 , 将来再发生病毒变异 , 我们在1-3个月内就能开发出新的疫苗 。
南都:这款一代苗可以应对奥密克戎变异株吗?
张必良:目前我们还未针对一代苗开展这方面的研究 , 不过针对德尔塔变异株的二代苗对奥密克戎变异株有一定的保护效果 , 三代苗则对目前所有变异株有显著的保护效果 。 赶在今年春节前 , 我们向CDE提交了二代苗的临床试验申报 。
南都:您对此次的临床试验有何预期?
张必良:原本一代苗需要完成临床Ⅰ期后再进行Ⅱ期试验 , 考虑到这个过程比较长 , 今年春节前我们向CDE申请同步交叉启动Ⅱ期试验 。 2月10日 , CDE批准了我们的申请 。 因此 , 我们的临床Ⅰ/Ⅱ期预计能提前完成 , 之后将到国外开展Ⅲ期试验 。
mRNA疫苗生产基地将于4月试投产
一年可生产4亿多剂疫苗
南都:锐博生物在广州科学城建设了寡核苷酸药物和mRNA创新性疫苗研发及生产基地 , 目前进展如何?
张必良:这就要说回到锐博的主业 。 锐博生物成立于2004年 , 主攻寡核苷酸药物产品研发和生产 , 2006年诺贝尔生理学或医学奖得主克雷格·梅洛(Craig Mello)是锐博生物的创办人之一 , 他是第一位走入广州民企的世界级科学家 , 在1998年与斯坦福大学Andrew Fire教授因发现RNA干扰技术(RNA interference , RNAi) , 获得了诺贝尔奖 。
我们在2012年启动建设了国内首条寡核苷酸GMP生产线 , 2016年获得药监局颁发的“药物生产许可证” , 填补了国内空白 。 从2018年上市第一款RNAi核酸药 , 至今在国外已有5款RNAi核酸药产品上市 。 由于业务发展很快 , 特别是第一款RNAi核酸药上市 , 我们马上启动了大规模原料生产基地建设项目 。

文章图片
锐博生物的mRNA疫苗GMP生产区 。 受访者供图
2020年底我们完成了国内首条mRNA疫苗GMP中试生产线的建设 , 至今已完成了10批次的mRNA疫苗生产 。 去年广州开发区投资引进了我们新成立的、专门从事创新药的阿格纳生物制药公司 , 并启动建设大规模的mRNA疫苗生产线 。 原本基地主要用于研发和生产寡核苷酸药物 , 因为新冠疫情 , 极大地推动了mRNA疫苗新技术路线的发展 , 并且mRNA创新性疫苗前景广阔 , 因此公司大力发展这项业务 。
目前 , 疫苗生产基地的设备已基本到位和调试完成 , 我们预计在3月份开展整体调试与验收 , 计划4月份启动试投产 , 届时将可大规模生产mRNA疫苗 。
南都:mRNA疫苗生产线规模有多大?
张必良:这应该是目前中国最大的mRNA疫苗生产基地 , 两层楼、共计5600平方米 , 有两条不同的生产线 , 一条是预灌充针生产线 , 另一条是西林瓶生产线 , 预计一年可灌装4亿多剂疫苗 。 两条生产线是全自动化的 , 从进料、灌装到包装一条龙打包好 , 可以直接送上冷链运输车 。
更为重要的是 , 经过多年核酸药物生产经验积累 , mRNA疫苗生产的原材料均实现了国产化 , 其中大部分核心原材料 , 锐博可以自产 , 因此能够大力加快我们疫苗的研发和生产 。

文章图片
锐博生物的mRNA疫苗灌装线 。 受访者供图
南都:可以说 , 新冠肺炎让锐博生物创造了一次发展新机遇 。
张必良:是的 。 新冠肺炎使mRNA疫苗产业化提前了十年 , 为了应对像新冠肺炎这样的重大暴发性公共卫生事件 , mRNA技术遇上了新机遇和发挥了它的安全性、快速性和高效性的优势 , 使得能在国外很快获得批准上市 。
锐博生物在RNA领域18年的沉淀 , 我们的mRNA生产经验和递送技术在千载难逢的机会中可以发挥作用 , mRNA是一种新技术路线的疫苗平台 , 不仅可以研发新冠疫苗 , 还可以开发流感、肿瘤等其它不同疫苗 。
加快推进疫苗海外临床及上市
引领大湾区乃至广东疫苗产业发展
南都:您是如何看待疫苗在应对新冠疫情全球化发展所产生的作用?
张必良:疫苗接种是预防和控制传染病最有效的公共卫生干预措施之一 。 相对于传统疫苗 , mRNA疫苗开发生产的快速性可填补新出现的大流行传染病与有效疫苗供应之间的空白 。
我认为 , 尽管如今有多个国家陆续宣布对外开放边境 , 但并不意味着新冠病毒即将消失 。 因为新冠病毒已属于全球性病毒 , 很难完全消灭 , 再就是有报道指出新冠病毒能在动物间传播 , 这就更难控制 。 现阶段 , 我们直面的更大挑战是病毒变异 , 谁都无法预测下一个变异病毒是什么 , 例如德尔塔病毒株和奥密克戎病毒株之间就没有任何关联性 , 而现有上市的疫苗并非对任何变异病毒都有效 。 如此看来 , mRNA疫苗确实非常重要 。
倘若新冠病毒不消失 , 我们就会像面对流感一样 , 每年都需要打疫苗 。 所以疫苗对于人民生活和国家经济发展也非常关键 。
南都:锐博生物的mRNA疫苗研发及生产基地 , 会为广东疫苗产业带来哪些新突破?
张必良:目前来看 , 在粤港澳大湾区乃至整个广东省都没有这么成熟的大规模生产基地 , 这个项目将发挥产业发展引领作用 , 并满足未来广东对于mRNA疫苗的需求 。
经过两年多的攻关 , 我们打破了许多技术壁垒 , 包括通过自主研发取代国外进口原材料 , 优化提升mRNA的递送技术 , 开发出肌肉注射的递送系统等等 , 积累了很多产业化的发展经验 。 尤其是疫苗能够保存在2℃至8℃的常规冰箱中 , 将更有利于帮助“一带一路”沿线国家中较落后国家或地区解决疫苗接种问题 。 本地化生产所带来的低成本优势 , 也将提高我们的全球化竞争力 。
此次新冠肺炎也进一步证明了mRNA技术的安全性和有效性 , 全球不少大型生物药企纷纷布局mRNA技术 , 不仅是疫苗产业 , 还包括细胞治疗、基因编辑等治疗手段 , 也有可能成为抗体取代性治疗 , 其应用领域将十分广泛 。 我们刚开始认为这只是颠覆了疫苗行业 , 如今看来 , 它将会颠覆整个生物医药行业 。
南都:接下来 , 新冠mRNA疫苗生产还会面临困难吗?
张必良:要推动疫苗的海外临床试验以及未来上市 , 困难还是难免的 , 最大的困难仍在于和时间“赛跑” 。 包括涉及一系列的行政审批流程 , 需要更多地与政府相关部门交流 , 争取政府层面的更大支持 。 广州将来要建成国际化一流城市 , 科学技术水平也要赶超其他国际大都市 , 我们希望能通过此次研发新冠mRNA疫苗 , 对社会贡献一份力量 。
采写:南都采访人员 莫郅骅
【海归张|广州产新冠mRNA疫苗临床满月!海归张必良团队答卷苗苗苗】图片:受访者提供
推荐阅读
- 人物|大学生为返校从山东骑车10天到上海:初二就出发了
- 施工|天津港航工程有限公司成功研发建造国内首座1200吨自升式海上施工平台
- 数字化|上海检察机关打造数字化智能监管平台 实现非羁押人员云监管
- 配置|助力跨境电商出海 腾讯云推出“轻量化”解决方案
- 功能|SK海力士开发出具备计算功能的内存技术“PIM”
- IT|由上海工厂生产的右舵版Model Y正式登陆英国 开始大批量交付
- 硬件|SK海力士宣布下一代GDDR6-AiM计算存储芯片
- 方解石|这种“疯狂”结构让海星灵活又坚固
- 台湾|视频|穿越海峡的新春祝福
- 芯片|SK海力士开发出下一代智能内存芯片技术PIM







