
文章图片

文章图片
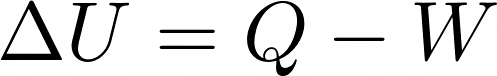
文章图片

文章图片

文章图片
麦克斯韦恶魔是一个思想实验 。 麦克斯韦在一封给他朋友的信中讨论了他的思想实验 。 此外 , 麦克斯韦还出版了一本名为《热的理论》的热力学书 , 在这本书中 , 他分享了他的思想实验 。 这个思想实验违反了热力学第二定律 , 这意味着系统的总熵要么增加 , 要么保持不变 。 1874年 , 威廉·汤姆森将这个思想实验的名字改为“麦克斯韦的恶魔” 。
在讨论麦克斯韦的思想实验之前 , 我们先来温顾一下热力学定律 。
热的动力学及其与物质的相互作用可以用热力学的四个定律来解释 。 温度是物质的热力学特征 , 而热是一种热能流 , 从高能介质流向低能量介质 。
- 热和温度概念的区别
热力学第零定律的重点是热平衡 , 即任何两个相关系统之间没有温差 。 温度是一个可测量的量 。 考虑三个孤立的系统 , 我们将它们称为A、B和C 。 首先 , 在A和B之间放置绝热体物质以防止它们之间传热 , 并在A、C之间放置导热体以允许A与C之间传热 。 因此 , A和B必须同时与C达到热平衡 。 那么 , A和B是否处于热平衡状态?为了找到答案 , 我们将导热材料转换为绝热体 , 然后测量A和B系统 。 实验证明 , A和B之间不会有任何传热 。 因此 , A系和B系之间存在热平衡 。
- 第0定律实验示意图
热力学第一定律
第零定律:如果两个热力学系统彼此之间处于热平衡状态 , 同时又分别与第三个系统处于热平衡状态 , 那么这三个系统彼此之间也处于热平衡状态 。
热能守恒(能量守恒)是用热力学第一定律来解释的 。 热量和功的差等于系统能量的变化量 ,
分子之间的结合能被解释为热力学能 。 例如 , 当你拿起一个物体来增加它的势能时 , 分子没有变形 , 因此不会改变物体的热力学能 。
热力学第一定律是能量守恒的一个广义概念 。 然而 , 这种能量是热能 , 它与系统传递的功和热有关 。 正因为如此 , 我们把它称为热力学能量守恒 , 这表明整个热力学能量的总量在宇宙中随着时间的推移总是恒定的 。 虽然热力学能不能在宇宙中产生 , 但它可以转化为各种形式的能量 。
热力学第二定律
第一定律:能量守恒定律规定任何孤立系统的总能量是恒定的;能量可以从一种形式转化为另一种形式 , 但既不能创造也不能毁灭 。
热力学第二定律解释了为什么所有的热力学过程都只能以某种方式进行 。 所有的机械能都转化为热能 。 例如 , 汽车突然刹车 。 车辆所做的机械功等于车轮产生的热量 。 然而 , 目前还没有办法把热能完全转化为机械能 。 将所有的热量转化为机械能将导致能量损失(摩擦) 。
- 转化为机械能的热能
第二定律还有一个表述 。 鲁道夫·克劳修斯提出了克劳修斯命题 , 该命题认为热量不会自发地从较冷的区域转移到较热的区域 。 因为 , 第一定律没有指出热量的方向 。 因此 , 第一定律和第二定律是相互独立存在的 。
熵是解释第二定律的一个关键概念 。 第二定律的熵解释是 , 每一个孤立系统的熵要么随时间增加 , 要么保持不变 。 熵准则的最佳解释是有多少能量分散到系统中 。 在任何孤立系统中 , 熵总是通过许多过程而增加 , 如热传递或热转换为不同形式的能量 。 熵减小的过程类似于看倒着播放的电影 。 那为什么熵在每个孤立系统中都趋于增加呢?可能是由于能量的本质 , 它倾向于在任何时候都扩散到整个宇宙 。







