AbMole科研-由于巨噬细胞c-Src信号传导增强TG2的缺失对胰岛素抵抗敏感
【|AbMole科研-由于巨噬细胞c-Src信号传导增强TG2的缺失对胰岛素抵抗敏感】
文章图片
AbMole精研抑制剂十年 , 最新的科研动态不断与您分享 。 本期与您分享的是:由于巨噬细胞 c-Src 信号传导增强 , 转谷氨酰胺酶2的缺失对饮食诱导的肥胖相关炎症和胰岛素抵抗敏感 。
转谷氨酰胺酶 2 (TG2) 是一种多功能蛋白质 , 可促进作为整合素β3辅助受体的凋亡细胞的清除(胞吞作用) 。 越来越多的证据表明 , 有缺陷的胞吞作用有助于慢性炎症性疾病的发展 。 肥胖的特征是脂肪组织中死亡的脂肪细胞和炎性巨噬细胞的积累 , 导致肥胖相关的代谢综合征 。 在这里 , 我们报告说 , 从骨髓衍生细胞中丢失 TG2 会使高脂肪饮食 (HFD) 诱导的病理变得敏感 。 我们发现代谢激活的 TG2 无效巨噬细胞表达更多的磷酸化 Src 和整合素 β3 , 出人意料地通过溶酶体胞吐作用更有效地清除垂死的脂肪细胞 , 但比野生型产生更多的促炎细胞因子 。 使用 LXR 激动剂进行抗炎治疗后 , 在骨髓衍生细胞中缺乏 TG2 的小鼠中 , HFD 诱导的表型发生逆转 , 与野生型小鼠相比 , 肝脏脂肪变性更少 , 证明脂质清除能力增强 。 因此 , 推测 LXR 激动剂治疗与增强溶酶体胞吐作用是否可以成为肥胖症的有益治疗策略是很有趣的 。
GW3965(Abmole , M1929 , 纯度99.46%)被用于对于体内 LXR 配体治疗 , 小鼠在骨髓移植后喂食 HFD 补充剂 20 mg/kg/天 。
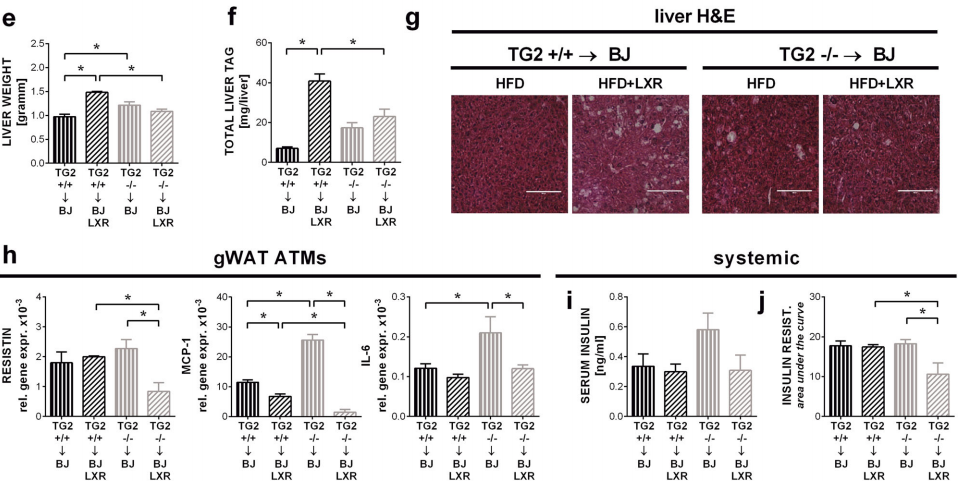
Fig. 5 LXR agonist treatment reverts HFD-induced obesity with less hepatic steatosis in mice lacking TG2 in the bone marrow- derived cells.
如前所述 , 我们将骨髓移植小鼠在其骨髓衍生细胞中表达或不表达 TG2 暴露于 LXR 激动剂 GW3965 , 在整个喂养期间与它们的高脂肪食物混合 。与之前的出版物 42 一致 , LXR 激动剂治疗阻止了 HFD 暴露小鼠的身体(图 5a)和性腺脂肪重量(图 5b)增加 。
鸣谢:Tibor Sághy et al. Cell Death Dis. 2019 Jun 5;10(6):439.
推荐阅读
- 又靓又能做科研,这位博士小姐姐,发完Science发Nature!
- 我国建造月球国际科研站,需突破一项关键技术,嫦娥四号差点实现
- 水不溶性药物由于溶解度低需要大量有机增溶剂,容易导致不良反应
- 由于纳米晶体药物不具有生物等效性,因此这些产品被视为“新药产品”
- 不惧“异变”,王亚平再创太空历史!辛苦科研每人获奖100万
- 年轻人想做好科研,最好不要太聪明
- 居里夫人:一个伟大的女科学家,搞科研的同时如何兼顾女儿的培养?
- 探秘首支新冠药物研发团队,他们是与病毒变异较量的科研人
- 科研动态:科学家解析早期地球上非生物世界进化的奥秘
- 由于使能技术的发展加速,通过质谱法对蛋白质进行分析变得越来越重要







