
文章图片
一、对酚酞的认识
1、酚酞是一种常用酸碱指示剂 , 广泛应用于酸碱滴定过程中 。 通常情况下酚酞试液是酚酞的乙醇溶液 , 在酸中呈现无色 , 在中性液中呈无色 , 在碱中变红色 。
2、酚酞是一种弱有机酸 , 在pH<7的溶液里为无色的内酯式结构 , 大于7时为红色的醌式结构 。
3、酚酞的变色范围是8.2~10.0 , 所以酚酞只能检验碱而不能检验酸 , 只能变成一种颜色 。
二、对使用酚酞试剂时几个现象的解释
使用酚酞试剂时常遇到下列几个现象:
1、在水中滴入酚酞后 , 会出现混浊现象 。 此现象产生的原因是酚酞滴入太多或试液过浓 。 因为酚酞是白色或微带黄色的细小晶体粉末 , 几乎不溶于水 , 易溶于酒精等有机溶剂中 , 因此通常制成1%的酒精溶液使用 。 由于酒精和水可以无限制地互溶 , 因此过多的酚酞试液滴入水中时 , 大量的水把酒精稀释了 , 降低了酚酞在酒精中的溶解度 , 酚酞便析出来了 , 这就产生了白色沉淀 。 因此 , 使用时一般滴加2—3滴 , 看清现象即可 。
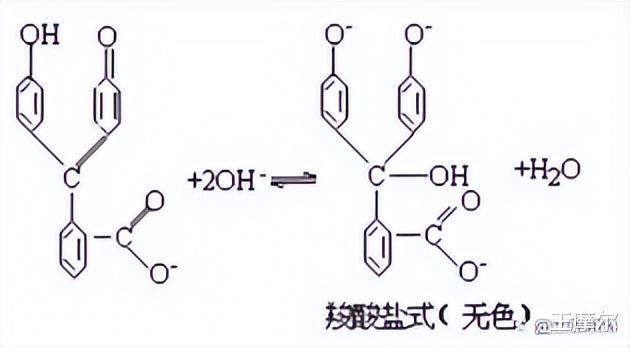
【使用酚酞指示剂的几个现象的解释?】2、在碱液中滴加酚酞试液时 , 开始溶液显深红色 , 在很短的时间内即变成浅红色至无色 。 其原因是碱液过浓 , 酚酞遇到较浓的碱液 , 会立即转变成无色的羧酸盐 , 生成酚酞二钠盐 , 这时酚酞的分子结构上出现醌基而显红色 。
但在过量的碱液中 , 酚酞二钠盐分子结构中的醌基变为苯环 , 出现醇式结构而生成酚酞的三钠盐 , 这时红色便消退了 。 所以 , 酚酞试剂滴入浓碱液时 , 酚酞会变成红色 , 很快红色退去变成无色 。
3、若将有酚酞的微碱性溶液放置一会儿 , 红色也会减退 。 这是因为此溶液吸收了空气中的CO2 , 使溶液的碱性减弱的缘故 。
2NaOH+CO2=Na2CO3+H2O
NaOH+CO2(过量)=NaHCO3 ,
NaHCO3溶液的PH在9左右 , 而酚酞的PH变色范围在8--10之间 , 酚酞溶液在PH=9左右时为无色 。 同时过量CO2与水反应 ,
CO2(过量)+H2O=H2CO3 ,
H2CO3与碱溶液中和至酸过量 。 因此 , 颜色最终由红色变为无色 。
4、在做中和滴定实验时 , 常用酸滴碱 , 若待测的碱(氢氧化钠)液浓度较大时 , 滴加酚酞试液 , 溶液立即显红色 , 随之变浅直到无色 。 此时若将标定的盐酸滴入待测的碱液 , 则溶液发生浅红→深红→浅红一系列的变化 。 (原因同2)
推荐阅读
- 看到中国月球车的车辙,美国登月再被质疑,为何美国月球车没有痕迹?
- 美国阿尔忒弥斯登月任务又又又推迟
- 世界上五类最大的鳄鱼,排名第一的是地球上最大的行动物
- 又漏了!好不容易修好的SLS登月火箭再次出故障,星舰也不容乐观
- 美国又要抄作业了:月球着陆器山寨嫦娥三号,事关登月成败
- 苏联航天员科马洛夫,升空前已知晓自己回不来,遗骸只剩一根足骨
- 长15米重达一吨,曾为地球霸主,吉尼斯纪录中最大的蛇—泰坦蟒
- 我国火箭研发科学家都承认美国人登月了,至今还有喷子不承认人家的优秀
- 快搭乘数字火箭,跟随《和平精英》一起飞向宇宙!







