文章图片

文章图片
文章图片
目前针对慢性脊髓损伤 (SCI) 的药物或物理康复疗法有限 , 主要集中在调节与慢性SCI相关的症状 , 如疼痛和/或肌肉痉挛 。 除了旨在优化损伤下方皮节运动控制的神经转移程序外 , 不存在可导致慢性脊柱创伤患者的运动或感觉功能临床相关改善的疗法 。
在过去的3年中 , 大量临床前数据表明 , 基于细胞替代的疗法对治疗各种脊髓神经退行性疾病具有有益的功能效应 。 在大多数实验中多数采用多能神经前体 (NPC) 来源于动物或人类胎儿中枢神经系统 (FT) 、胚胎干细胞 (ESC) , 或诱导多能干细胞 (iPSC)已用于体内脊髓移植 , 导致有丝分裂后神经元、星形胶质细胞和少突胶质细胞的数量因NPC来源而异 。 由于FT衍生的NPC已确定的谱系潜力和缺乏畸胎瘤形成 , 它们具有最有利的安全性 。
NSI-566系是FDA授权进行临床试验的人类神经干细胞系 。
NSI-566神经干细胞系:NSI-566是一种人脊髓源性神经干细胞系 。 神经干细胞是哺乳动物胎儿发育过程中沿神经轴存在于神经上皮中的前体细胞 。 NSI-566来源于一个8周胎龄胎儿的脊髓 。
该组织是根据美国国立卫生研究院 (NIH) 和食品和药物管理局 (FDA) 良好组织实践指南以及外部独立审查委员会批准的协议获得的 。 神经干细胞通过分离下颈椎/上胸椎区域的单片脊髓组织并将其扩展为单行来分离 。
神经干细胞移植治疗慢性脊髓损伤的首次人体I期研究
虽然NSI-566神经干细胞系在ALS患者完成的I期和II期临床试验中显示出良好的安全性 , 尚未评估其安全性、耐受性和支持进一步用于SCI患者的概念验证数据 。 历史临床数据表明 , 损伤后1周稳定的完全性SCI (ASIA-A) 患者在损伤水平以下一个皮节发生自发感觉改善的机会不到2% 。
在这里 , 我们报告了第一批患者的结果 , 该患者参加了将神经干细胞产品NSI-566植入慢性ASIA-A级胸部SCI患者的损伤部位的I期首次人体临床试验 。
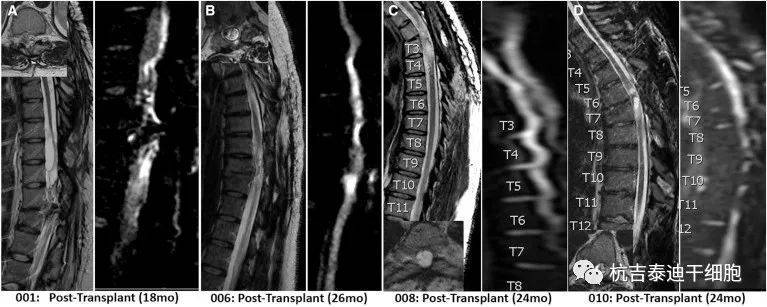
神经干细胞移植治疗慢性胸椎SCII期临床试验共有四名受试者接受了NSI-566脊髓植入术 , 术后随访时间为18至27个月(表1) 。 所有受试者都很好地耐受了该程序 , 在程序后期间没有严重的不良事件 。 已收集前瞻性数据 , 包括ISNCSCI评分、功能和疼痛调查、SCIM评分、肌电图 (EMG)、脑运动控制评估 (BMCA) 和系列MRI 。 还定期监测供体特异性HLA抗体的存在 。
表1患者特征
【神经干细胞移植治疗慢性脊髓损伤的人体I期研究】表1
注射细胞方式:使用浮动插管技术在双侧进行3次注射 , 每位受试者总共进行6次注射(注射体积为2×105个细胞 , 每次注射10uL) 。
临床试验一:参与该研究的第一位患者是一名26岁女性(受试者001) , 在机动车事故后有T8神经损伤水平 。 神经干细胞植入后 , ISNCSCI神经系统评估显示 , 与治疗前相比 , 在6、12和18个月时双侧感觉和运动改善了两级(从T8到T10) , 在27个月时感觉和运动改善了一级基线 。
此外 , BMCA在下肢显示出新发展的肌肉对强化动作的反应 。 这种改善在细胞移植后18至27个月内出现 , 没有证据表明在3、12、18或27个月时循环抗供体HLAI类或I类抗体(图3A-3D) 。
图3大脑运动控制评估 (BMCA) 和EMG评估以识别自愿或强化机动启动的EMG活动
(A和B)自愿或强化机动触发的BMCA活动的记录显示在受试者001(4.4.2016示踪剂)细胞移植后18个月没有可检测到的BMCA反应 。
(C和D) 在移植后27个月进行的后续记录显示 , 在强化操作 (D) 后 , 小腿三头肌出现EMG反应 。 在任何一项研究中(C) , 都没有注意到左脚踝跖屈或背屈的自主尝试 。 与之前的记录相比 , 红色箭头显示小腿三头肌的新活动 , 增强动作(颈部屈曲和深呼吸);水平黑条表示起始标记 。
(E和F)受试者006右侧T6椎旁肌的EMG记录 。 与基线记录相比 , 在细胞移植后12个月记录了多个新的运动单位(红色箭头) 。
(G和H)受试者010的T6和T7椎旁肌的EMG记录 。 与基线(12周)记录相比 , 在从T7椎旁肌移植细胞后6个月和18个月记录了一个新的运动单元(读取箭头) 。推荐阅读
- 四川绵竹上空出现大量蝙蝠群,有可能是地震的前兆吗?
- 月球是一颗人造卫星?列举科学家探测数据,证明月球是空心的
- 从科学的角度探讨修仙能不能实现,我认为可行!
- 转基因食物,从“反自然”到“自然”
- 人类在火星上发现奇怪、难以置信的6个物体!
- 一项在确定粒子和细胞如何产生大规模动态方面的新研究取得了进展 正在揭开被称为“时间箭头”的这个谜团
- 从气味到行动——气味如何在大脑中处理并影响行为
- 大脑是如何处理视觉区域传回来的信息的?
- 人的四大物质构成,如何让人拥有“自我”的能力?







